El desarrollo y la producción de vacunas en tiempos de pandemia
Ante la magnitud de la pandemia de la COVID-19, la creación de una vacuna eficaz y bien tolerada se ha convertido en un gran reto internacional.
El acelerado desarrollo de una vacuna frente al SARS-CoV-2 se basa en el profundo conocimiento de las diferentes tecnologías de producción de vacunas, los avances científicos y la cooperación mundial.
Las autoridades sanitarias nacionales y europeas han adaptado sus sistemas reglamentarios para acelerar, en la medida de lo posible, el desarrollo de posibles vacunas y han publicado recomendaciones dirigidas a los laboratorios cuyo objetivo es garantizar la ética y la validez científica de los estudios clínicos1.
Retos para la creación de una vacuna durante la pandemia
Dada la enorme repercusión de la COVID-19 en el mundo, era indispensable desarrollar las vacunas en el menor tiempo posible. Sin embargo, su creación se enfrentó a numerosos y complicados retos:
-
Por lo que respecta a la eficacia, las posibles vacunas debían producir una inmunidad sólida2. La elección de la plataforma de la vacuna y el diseño del antígeno suponía un gran desafío3.
-
Además, las vacunas debían ser bien toleradas y cumplir todos los requisitos de seguridad. Para ello se estudia previamente la tolerancia en modelos animales adecuados y se somete a una estricta vigilancia la seguridad de las posibles vacunas durante los ensayos clínicos3.
-
Por último, en el plano estratégico y logístico, las vacunas tenían que ser fáciles de producir y su despliegue a gran escala debía poder realizarse de manera rápida y ágil2.
El desarrollo de posibles vacunas frente a la COVID-19 se aceleró gracias a los profundos conocimientos sobre la producción de vacunas adquiridos en anteriores procesos.
Además, dado que el SARS-CoV-2 es parecido a otros coronavirus (SARS-CoV-1 y MERS-CoV) que ya se habían investigado anteriormente, la búsqueda de vacunas frente al SARS-CoV-2 no partió de cero4.
Algunas plataformas de vacunas (por ejemplo, las basadas en el ARN) ofrecieron un gran potencial de desarrollo rápido (más información en la página “Tecnologías de las vacunas”), mientras que otras dependen de vacunas ya existentes o en desarrollo dirigidas a otras enfermedades, por lo que puede que ya se dispusiese de algunos de los datos de seguridad necesarios3.
Asimismo, el intercambio de conocimientos científicos a nivel internacional también permitió reducir el tiempo necesario para completar todas las fases de desarrollo de una vacuna frente a la COVID-194.
Tiempo de desarrollo de una vacuna tradicional frente al desarrollo en pandemia
El desarrollo tradicional de una vacuna puede durar años, a veces una década o incluso más. Sigue una progresión lineal que comprende desde la identificación de la diana de la vacuna a la realización de una serie establecida de ensayos clínicos de fase I, II y III basados en la evaluación de la probabilidad de éxito en cada etapa3.
En el “modelo convencional”, la producción de vacunas a gran escala no se inicia hasta que el nivel de certeza de la seguridad y la eficacia de la posible vacuna es elevado3.
Proceso del desarrollo de vacunas a las necesidades de la pandemia5.

Creado a partir de la Agencia Europea de Medicamentos
En cambio, en el “modelo pandémico” buena parte de esos procesos se realizan en paralelo en vez de secuencialmente. El desarrollo de la producción, la producción de cantidades comerciales y el aumento de la capacidad logística de distribución de la vacuna pueden realizarse al mismo tiempo que se llevan a cabo los ensayos clínicos3.
De este modo, la producción a gran escala puede iniciarse de inmediato una vez se confirma la eficacia y la seguridad de la vacuna, o incluso antes3.
Sin embargo, este modelo conlleva un riesgo considerable para los laboratorios que desarrollan la vacuna, puesto que la producción a gran escala, la planificación logística y otros elementos clave necesarios para la comercialización de la vacuna tienen lugar antes de que se confirme su eficacia3.
Proceso del desarrollo de vacunas a las necesidades de la pandemia5.
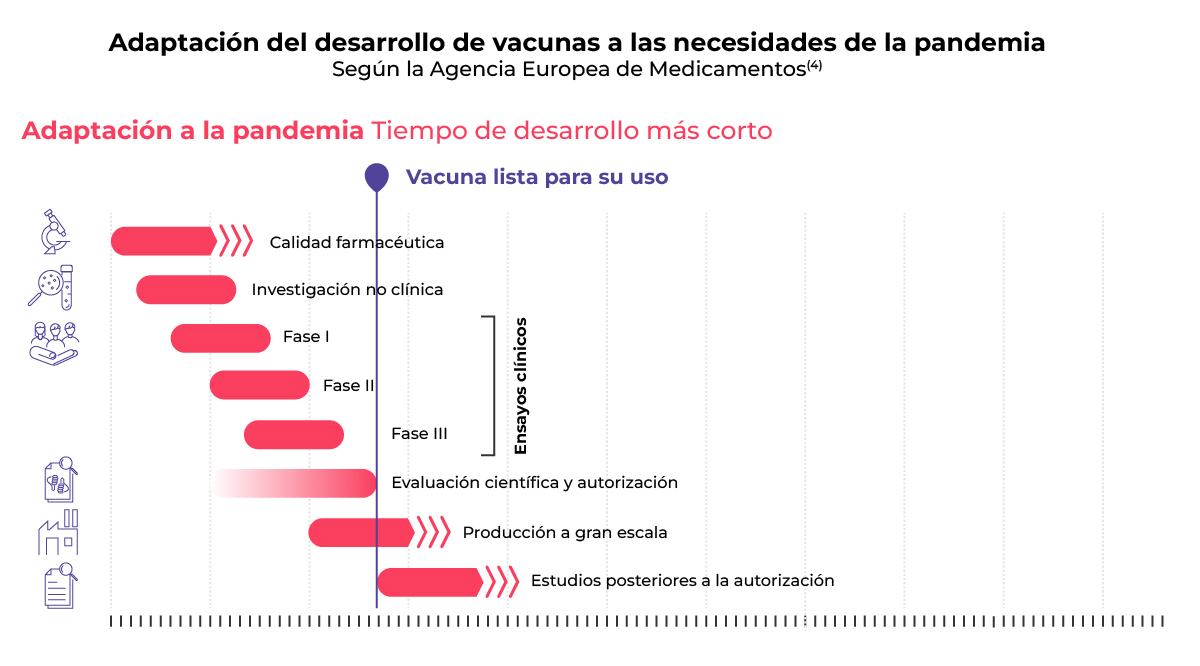 Creado a partir de la Agencia Europea de Medicamentos
Creado a partir de la Agencia Europea de Medicamentos
Las fases de desarrollo de una vacuna
Normalmente, el desarrollo de una posible vacuna sigue un proceso dividido en tres grandes etapas:5
-
Estudios preclínicos (cultivo celular in vitro y en animales in vivo).
-
Ensayos clínicos de fase I, II y III en humanos que permiten evaluar la seguridad, determinar la dosis más adecuada y demostrar la eficacia y la seguridad de la posible vacuna a gran escala.
-
Evaluación científica del expediente de registro para la autorización de comercialización (AC) de la vacuna por parte de las autoridades sanitarias. La producción de la vacuna pasa a ser a gran escala una vez obtenida la autorización de comercialización y posteriormente la vacuna se pone a la venta en el mercado5.
En una situación de pandemia, muchas de las fases se solapan. Las fases de los ensayos clínicos también pueden agruparse en un mismo estudio (por ejemplo, fase I/II o II/III). La adaptación de la capacidad de producción se realiza de forma simultánea a los ensayos clínicos y a veces la producción a gran escala comienza incluso antes de que finalicen5. La vacuna puede empezar a estar lista para su comercialización en cuanto se obtenga la AC5.
Acceda aquí a las recomendaciones sanitarias y de salud pública de interés general del Ministerio de Sanidad sobre la COVID-19
PP-CMR-ESP-0232
Bibliografía
-
European Medicines Agency. Fast-track procedures for treatments and vaccines for COVID-19. Fast-track procedures for treatments and vaccines for COVID-19 - infographic Respuesta común de la UE a la COVID-19 | Unión Europea (europa.eu) Consultado en septiembre de 2024
-
Funk CD, Laferriere C, Ardakani A. A snapshot of the global race for vaccines targeting SARS-CoV-2 and the COVID-19 pandemic. Front Pharmacol. 2020; 11:1 -17.
-
Lurie N, Saville M, Hatchett R, et al. Developing COVID-19 vaccines at pandemic speed. N Engl J Med. 2020;82;1969-1973.
-
Organisation for Economic Coopération and Development. Treatments and a vaccine for COVID-19: the need for coordinating policies on R&D, manufacturing and access - 29 de mayo de 2020. Treatments and a vaccine for COVID-19: The need for coordinating policies on R&D, manufacturing and access | OECD Consultado en septiembre de 2024
-
European Medicines Agency. Cavaleri M. How are COVID-19 vaccines developed? www.ema.europa.eu/en/documents/presentation/presentation-how-are-covid-19-vaccines-developed-marco-cavaleri_en.pdf Consultado en septiembre de 2024